Índice de Contenidos
Mastocitosis sistémica (MS)
La mastocitosis sistémica (MS) engloba un grupo heterogéneo de enfermedades con un denominador común: el crecimiento anormal de mastocitos clonales (mutados) y la acumulación, a lo largo del tiempo, de estas células en distintos tejidos y órganos del cuerpo [1–3]. La Comisión Europea de Salud Pública considera la MS una enfermedad “rara o poco frecuente”, con una prevalencia estimada de 1 caso por cada 10.000 habitantes [4]
La mutación D816V del gen KIT es la causante de la mastocitosis en la gran mayoría de los pacientes adultos y en el 30% de los pacientes pediátricos. El gen KIT ejerce un papel muy importante en la regulación de la síntesis de mastocitos, su proliferación y su supervivencia. En los pacientes con MS, como existe una mutación de este gen, existe un descontrol de estas funciones, generándose una mayor cantidad de mastocitos clonales (mutados, anormales) que además tendrán unas características y comportamiento diferentes al de los mastocitos normales (no mutados) [1–3]
La OMS clasifica las MS en 6 subtipos: la aislada de médula ósea, la sistémica indolente, la quiescente, la agresiva, la leucemia de mastocitos y la asociada a neoplasia hematológica [1,3].
Cada subtipo se define por unas características clínicas y diagnósticas distintas y asocian distintos pronósticos de enfermedad y supervivencia. La MS aislada de médula ósea, la sistémica indolente y la quiescente se consideran MS no avanzadas por su mejor pronóstico, mientras que los otros 3 subtipos se consideran MS avanzadas, con una afectación orgánica y pronóstico reducido en comparación con los anteriores (AKIN, VALENT). Afortunadamente, las MS no avanzadas constituyen la forma más frecuente de la enfermedad y representan más del 90% de todas las MS por lo que, en general, los pacientes con mastocitosis tienen un pronóstico favorable [1–3].
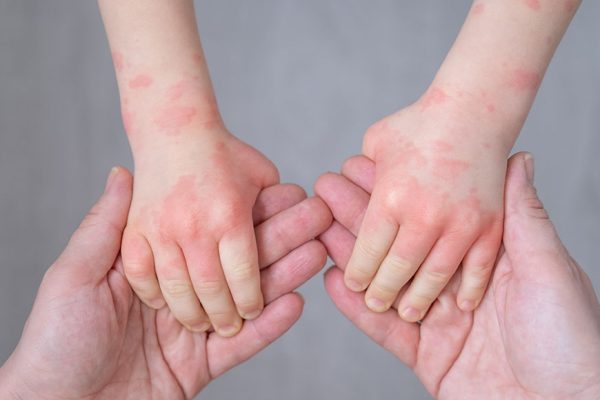
Al ser células del tejido conectivo, los mastocitos están presentes en prácticamente todos los órganos del cuerpo, especialmente debajo de la piel, alrededor de los vasos sanguíneos, el tracto gastrointestinal, el tejido nervioso y el tracto respiratorio. Así, las manifestaciones clínicas de las MS suelen ser muy heterogéneas, incluyendo desde la expresión cutánea (prurito con o sin erupciones, rubor facial), los síntomas gastrointestinales (dolor, pirosis, náuseas, diarreas), hasta los musculoesqueléticos (artralgias, mialgias), los neuropsiquiátricos (cefalea, embotamiento, trastornos depresivos) o los cardiovasculares (mareo, hipotensión, síncope) entre otros [1,3,5].
Las complicaciones más graves de la MS son, por un lado, la osteoporosis y las visceromegalias producidas por la acumulación e infiltración de los mastocitos a lo largo del tiempo, y por otro lado la anafilaxia, producida por una liberación rápida y masiva de mediadores mastocitarios, como la histamina y la triptasa, entre otros [1–3].
Mastocitosis sistémica y anafilaxia
La anafilaxia es una reacción potencialmente mortal, resultado de la activación sistémica de los mastocitos tras la exposición a un desencadenante, que se desarrolla de forma muy rápida (en segundos o minutos) y puede tener consecuencias fatales [6,7].
La evidencia científica sugiere que los pacientes con MS tienen un riesgo mucho mayor de anafilaxia en comparación con la población general, con una incidencia reportada del 20-49 %; mientras que en la población general la incidencia de anafilaxia es del 0.05 -2% [8,9].
Las anafilaxias idiopáticas (esto es, sin desencadenante identificable) y las inducidas por venenos de himenópteros son las causas más frecuentes de anafilaxia en pacientes con MS [9].
La adrenalina intramuscular es el único tratamiento que ha demostrado ser efectivo en el tratamiento de la anafilaxia [6,7], mientras que no existe evidencia científica sobre el beneficio de otros medicamentos comúnmente utilizados para estas reacciones (como los corticoides o los antihistamínicos) [7,10–12]. Por lo tanto, éstos constituyen alternativas de segunda o tercera línea. Adicionalmente, se ha demostrado que un retraso en la administración de adrenalina se asocia a un aumento de la mortalidad y complicaciones en los pacientes que sufren una anafilaxia, de modo que es imprescindible que la adrenalina se administre de forma inmediata cuando se desencadena una anafilaxia [6,7].
En este contexto, el autoinyector de adrenalina (AIA) resulta fundamental para el manejo de la anafilaxia. Se trata de un dispositivo precargado con una dosis de adrenalina que está diseñado para que cualquier paciente pueda administrarse el tratamiento precozmente, de una forma sencilla, segura, fácil, y sin necesidad de tener formación sanitaria.
En conclusión, la MS es una enfermedad rara que puede causar una amplia gama de síntomas y complicaciones, incluyendo la anafilaxia. La evidencia científica sugiere que los pacientes con MS tienen un mayor riesgo de anafilaxia, para la cual la adrenalina intramuscular es el tratamiento de primera línea. Finalmente, un retraso en la administración de adrenalina puede aumentar la morbimortalidad de la anafilaxia, de manera que la familiarización y el entrenamiento de los pacientes con MS y sus cuidadores principales en el uso de los AIAs es importante y necesario para prevenir y tratar las complicaciones de esta enfermedad.
Dra. Paula Vázquez Revuelta
Paula Vázquez Revuelta es médica especialista en Alergología con una amplia experiencia en el sector público y especial dedicación al ámbito de la desensibilización a fármacos antineoplásicos y las mastocitosis sistémicas no avanzadas, entre otros. Licenciada en Medicina y Cirugía por la Universitat Autònoma de Barcelona en el 2012, la Dra. Vázquez se especializó en Alergología en el Hospital Universitario Ramón y Cajal de Madrid en el 2017. Desde el año 2018 trabaja en el Servicio de Alergología del Hospital Univeristari Bellvitge, donde combina la asistencia a pacientes con alergia respiratoria y cutánea con la asistencia y coordinación de la Unitat de Dessensibilització a Fàrmacs OncoHematològics (UDFOH) del Institut Català d’Oncologia, en la cual se llevan a cabo los estudios y desensibilizaciones a los pacientes con cáncer y alergia a sus tratamientos antineoplásicos. Desde el año 2022, también es la responsable de la consulta monográfica de mastocitosis sistémicas no avanzadas del Servicio.
Dr. Ramon Lleonart Bellfill
Ramon Lleonart Bellfill es licenciado en Medicina y Cirugía por la Universidad Central de Barcelona (Hospital Clínico, 1986). Obtuvo el título de Médico Especialista en Alergia e Inmunología Clínica en 1990. Es facultativo especialista en la Unitat d’Al·lèrgia del Hospital Universitari de Bellvitge (L’Hospitalet de Llobregat) desde julio 2004. Jefe de Servicio de Alergología desde septiembre 2022. Ha participado en proyectos de I+D con entidades públicas y privadas, y tiene casi un centenar de publicaciones científicas. Es miembro del GEAB, Grupo Español de Estudio del Angioedema por Bradicinina, así como de la SCAIC, SEAIC, EAACI y AAAI. Áreas de especial interés: Angioedema hereditario y asma grave.